Aprobado el primer ensayo clínico de una vacuna española contra la COVID-19
La empresa Hipra ha recibido la autorización para el primer ensayo clínico de su vacuna PHH-1V
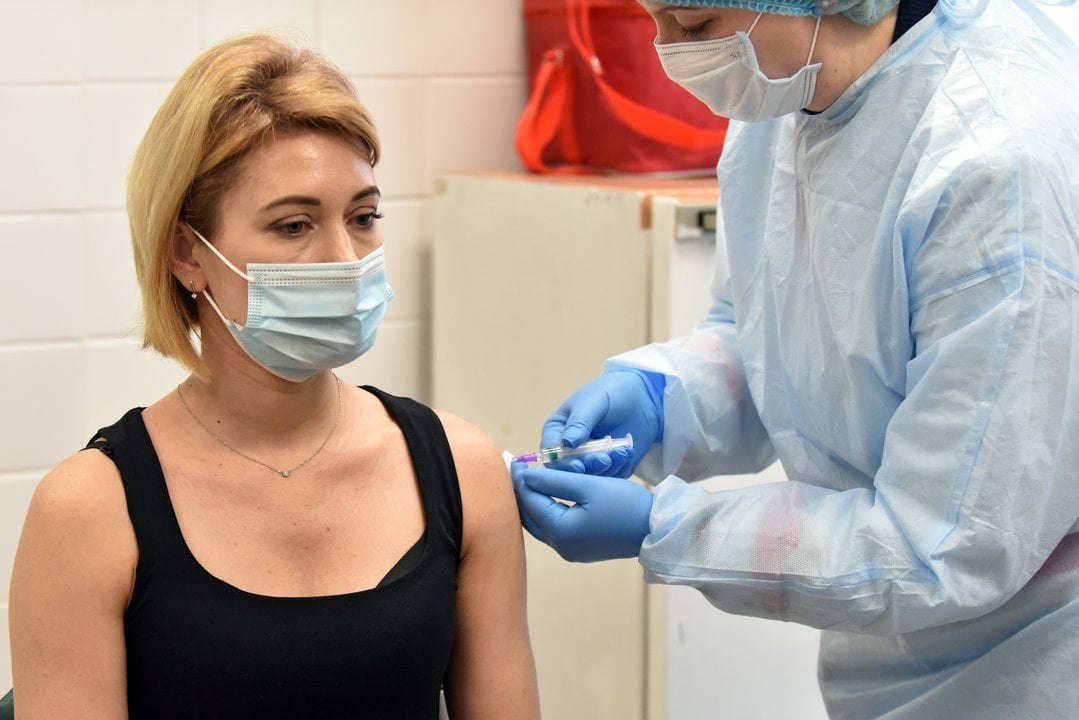
La compañía farmacéutica española Hipra ha recibido la aprobación por parte de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) para realizar el primer ensayo clínico de su vacuna PHH-1V contra la COVID-19.
Esta es la primera vacuna desarrollada en nuestro país que recibe la autorización para ser probada en humanos.
Los ensayos clínicos se realizarán de forma aleatoria, controlada y enmascarada. Esto quiere decir que el paciente y los investigadores no sabrán si se está administrando la vacuna de prueba (en fase I/II) o una de las vacunas autorizadas enmascarada. Mediante este ensayo se pretende analizar y estudiar la seguridad y la tolerabilidad de esta vacuna en primer lugar, y su inmunogenicidad y eficacia en segundo lugar.
"Esta vacuna está basada en dos proteínas recombinantes estructuralmente similares, una correspondiente a la variante alfa y otra correspondiente a la variante beta, que se unen formando una estructura única llamada dímero, y que se acompañan de un adyuvante que incrementa la respuesta inmunológica", explican desde la AEMPS.
Se realizarán los ensayos en grupos de voluntarios de entre 18 y 39 años, empezando con una dosis baja por diferentes grupos de cohortes y aumentándola una vez se hayan realizado las tareas de vigilancia y se haya comprobado que no hay problemas de seguridad. Posteriormente se irán aumentando las dosis, hasta encontrar la dosis óptima de la vacuna. Se realizarán dos inyecciones separadas en el tiempo por un plazo de 21 días.
"Durante todo ensayo se llevará a cabo una monitorización estrecha de todos los voluntarios y una identificación de todos los casos de acontecimientos adversos y de infección por SARS-CoV-2 que se vayan produciendo. Esto permitirá llevar a cabo análisis preliminares con datos intermedios que permitan continuar avanzando en la investigación", indican desde la Agencia Española de Medicamentos y Productos Sanitarios. Los datos y conclusiones finales se obtendrán una vez haya finalizado el ensayo.
La vacuna será, en su caso, autorizada, una vez se hayan cumplido todos los procedimientos y los estándares regulatorios que permitan su comercialización.







